EL ÁTOMO
De un modo más formal, definimos átomo como la partícula más pequeña en que un elemento puede ser dividido sin perder sus propiedades químicas.
El origen de la palabra átomo proviene del griego, que significa indivisible. En el momento que se bautizaron estas partículas se creía que efectivamente no se podían dividir, aunque hoy en dia sabemos que los átomos están formados por partículas aún más pequeñas, repartidas en las dos partes del àtomo, las llamadas partículas subatómicas.
Partes y estructura de un átomo
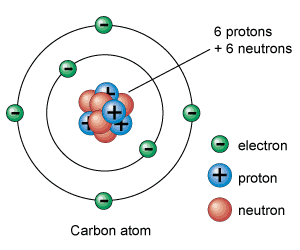
La estructura de un átomo resulta muy sencilla la cual la dividimos en dos partes: núcleo y corteza.
El núcleo es la parte central de la estructura del átomo. En la parte del núcleo se encuentran los protones (partículas con carga positiva) y los neutrones (partículas sin carga eléctrica).
En la corteza, la parte exterior del átomo se encuentran los electrones (partículas con carga eléctrica negativa).
Los protones, neutrones y electrones son las partículas subatómicas que forman la estructura del átomo. Lo que diferencia a un átomo de otro es la relación que se establecen entre ellas.
Los electrones, de carga negativa, son las partículas subatómicas más ligeras. Los protones, de carga positiva, pesan unas 1.836 veces más que los electrones. Los neutrones, los únicos que no tienen carga eléctrica, pesan aproximadamente lo mismo que los protones.
Los protones y neutrones se encuentran agrupados en la parte central del átomo formado el núcleo atómico. Por este motivo también se les llama nucleones.
De este modo, la parte central del átomo, el núcleo atómico, tiene una carga positiva en la que se concentra casi toda su masa, mientras que en el escorzo alrededor del núcleo atómico hay un cierto número de electrones, cargados negativamente. La carga total del núcleo atómico(positiva) es igual a la carga negativa de los electrones, de modo que la carga eléctrica total del átomo sea neutra.
Modelo de Bohr
Esta descripción de los electrones orbitando alrededor del núcleo atómico corresponde al sencillo modelo de Bohr. Según la mecánica cuántica cada partícula tiene una función de onda que ocupa todo el espacio y los electrones no se encuentran localizados en órbitas aunque la probabilidad de presencia sea más alta a una cierta distancia del núcleo.
Propiedades de los átomos
Las unidades básicas de la química son los átomos. Durante las reacciones químicas los átomos se conservan como tales, no se crean ni se destruyen, pero se organizan de manera diferente creando enlaces diferentes entre un átomo y otro.
Los átomos se agrupan formando moléculas y otros tipos de materiales. Cada tipo de moléculaes la combinación de un cierto número de átomos enlazados entre ellos de una manera específica.
Según la composición de cada átomo se diferencian los distintos elementos químicos representados en la tabla periódica de los elementos químicos. En esta tabla podemos encontrar el número atómico y el número másico de cada elemento:
- Número atómico, se representa con la letra Z, indica la cantidad de protones que presenta un átomo, que es igual a la de electrones. Todos los átomos con un mismo número de protones pertenecen al mismo elemento y tienen las mismas propiedades químicas. Por ejemplo todos los átomos con un protón serán de hidrógeno (Z = 1), todos los átomos con dos protones serán de helio (Z = 2).
- Número másico, se representa con la letra A, y hace referencia a la suma de protones y neutrones que contiene el elemento. Los isótopos son dos átomos con el mismo número de protones, pero diferente número de neutrones. Los isótopos de un mismo elemento, tienen unas propiedades químicas y físicas muy parecidas entre sí.








